米国 / シカゴにて5月31日から6月5日まで開催された米国臨床腫瘍学会 (American Society of Clinical Oncology: ASCO) は、過去最多となる4万人以上の医療関係者が参加し、大きな盛り上がりを見せていました。サイニクスからは5名、Oracle Life Sciencesからは総勢38人が参加しました。今回のSynix Oncology Newsletterでは参加したサイニクスのスタッフが学会の様子についてお届けします。
オンコロジースペシャリストのレポートはこちらから!
膵臓がんで初めてのバイオマーカー治療
膵臓がんは自覚症状が少なく進行が早いため、発見されたときにはかなり進行しているがん種となる。CancerMPact – Patient Metricsでは、Stage IVで診断される患者割合が日本で46%、米国では53%となっていて、その3割~4割の患者群が積極治療できない状況にある。
他のがん種では、分子標的薬や免疫療法といった新しい薬剤の使用オプションが加わってきているが、膵臓がんは、多くの薬剤開発で失敗してきた歴史がある。その中でTarcevaが生存率の延長をもたらした分子標的薬となっているが、2週間程の統計的優位を示す結果である。(Moore, J Clin Oncol, 2007)。これら実臨床の現状および薬剤開発の状況からも、膵臓がんは最もアンメット・メディカル・ニーズの高いがん種の一つと言えるだろう。
Late Breaking Abstractでは、 第lll相POLO試験より1次治療の白金系抗癌剤で増悪しなかったBRCA陽性の患者に対するPARP阻害薬 Lynparzaの維持療法が、主要評価項目のmPFSは7.4ヶ月(vsプラセボ 3.8ヶ月 HR 0.53)に達し、膵臓がんでは初めて特定バイオマーカーでの有効治療の可能性が示唆された。全生存期間(OS)の最終解析は今後となるが、現時点で18.9ヶ月 (vsプラセボ 18.1ヶ月)の結果となっており、今後の発表が注目される。(HS)

Oracle Life Sciences オンコロジースペシャリストのレポート
Lynparza is paving new ground in pancreatic cancer, aiming to establish a maintenance setting and patient segmentation based on a biomarker (gBRCA mt) in first-line metastatic disease
多様化する前立腺がんの治療選択と課題
前立腺がんの薬物療法はここ数年で激しく変化しており、日本においても2014年以降Xtandi (enzalutamide, Astellas)、Zytiga (abiraterone, Janssen)、Erleada (apalutamide / Janssen)等の次世代アンドロゲン剤の登場により多様化している。一方では使用のタイミング、最適なシーケンス、従来の化学療法への切り替え、バイオマーカーの特定など課題も残されており、今回のASCOでも多く議論されていた。
前立腺がんの薬物療法は「より早く」、「より強く」
今回のASCOでは大きな2つの発表があった。①転移性HSPCでXtandi + ADT療法を評価した第lll相ENZAMET試験、②非転移HSPCでErleada + ADT療法を評価した第lll相TITAN試験だ。どちらもPFS (無増悪生存期間)、OS (全生存期間)の延長が認められ、次世代アンドロゲン剤の早期導入が加速している。
非転移性CRPC領域においては、SPARTAN試験、PROSPER試験、ARAMIS試験等の大規模臨床試験結果から多くのエビデンスが報告されており、NCCNガイドラインではPSA倍加時間(PSADT)が10ヶ月以内の前立腺がん患者へ次世代アンドロゲン剤が強く推進されている。MFS (無転移生存期間) が改善している事から、早期ステージにおける有効な治療選択になることは間違いないが、薬物治療法の副作用によるQOL低下、早期ステージからの治療による超長期治療期間により発生する高額な医療費についても議論されていた。過剰診断・過剰治療を防ぐ為のPSA検査に変わる新たな診断検査の検討、ゲノム医療の需要がより増しそうだ。
転移性CRPCで進む新しい併用レジメンの開発 More is NOT Better?
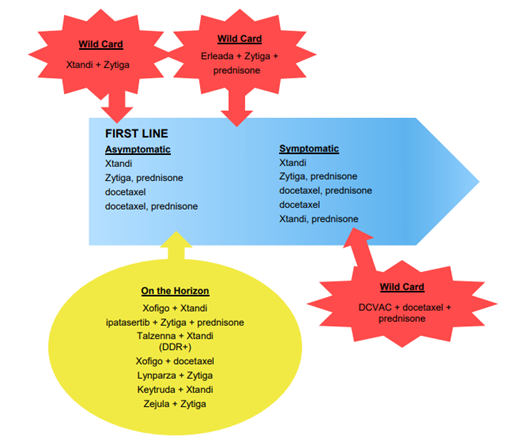
転移性CRPCでは新しい併用で次世代アンドロゲン剤の開発が進んでいる。今回のASCOではXtandi + Zytiga + Prednisoneの3剤併用療法を評価した第lll相Alliance A031201試験 (日本は未参加) 結果が発表されたが、主要評価項目である全生存期間(OS)の延長は達成せず、3剤併用群では有害事象の発生率も高くなる結果となっていた。日本でも次世代アンドロゲン剤2剤併用Erleada + Zytiga、AKT阻害剤との併用Ipatasertib + Zytiga、Xtandi + Xofigo等の新しい併用レジメンの開発が進んでいる。転移性CRPCにおける上乗せによる治療効果については、引き続き注目していく必要がありそうだ。
転移性CRPCのアンメット・メディカル・ニーズは延命治療よりもQOLの改善?
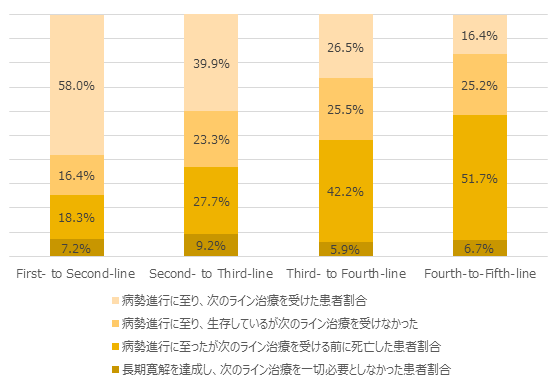
転移性CPRCの治療選択は増えているものの、転移性CRPC患者の半数は1次治療後に延命治療を受けていないとの後ろ向き研究も報告されていた。市場調査 (Treatment Architecture United States 2018) でも、1次治療を受けた患者の約35%が死亡または生存しているが次の治療を受けていない。この割合は後期ラインになるに伴い高くなっている。
転移再発させないために、早期ステージ薬剤開発におけるMFS(無転移生存期間)評価の重要性はもちろん、転移性前立腺がん患者の多くは骨転移を有しいている事から実臨床では疼痛管理、骨マネジメント等のサポーティブケアが重要であることも興味深かった。また早期治療後の予後/再発リスクはPSA倍加時間(PSADT)で大きく異なることからも、転移性前立腺がんにおけるPSA倍加時間別の治療戦略の重要性についても注目が集まっていた。 (NO)

Oracle Life Sciences オンコロジースペシャリストのレポート
Will Erleada take the lead in metastatic CSPC? New interim data at ASCO 2019 from the Phase 3 TITAN trial supports addition of Erleada to ADT for a broad range of patients in this setting.
新薬の登場が相次ぐ多発性骨髄腫
多発性骨髄腫は近年、Kyprolis (carfilzomib,Amegen/Ono)、Empliciti (elotuzumab, BMS)、Farydak (ponobinostat,Novartis)など特に再発・難治性の多発性骨髄腫における新たな薬剤の登場が相次ぎ、治療選択が急速に変化を遂げている。今回のASCOでは、今後のさらなる治療選択拡大の可能性を示唆する結果が多く発表された。
そして、「新たな」「広がる」選択肢・・・Darzalex vs isatuximab
日本では2017年9月に再発・難治性多発性骨髄腫で抗CD38モノクロナール抗体Darzalex (daratuzumab,GenMab/Janssen)が承認され、市場調査 (Treatment Architecture 2018) の結果でも、後期ラインでDarzalexを含むレジメンの浸透が確認されている。今回のASCOでは、Darzalexと同じ抗CD38モノクロナール抗体isatuximab (Sanofi)+Pomalyst+低用量dexamethasone (IsaPd)とPomalyst+低用量dexamethasone (PD)を比較した第lll相ICARIA-MM試験において、IsaPdがPDに比べてPFSを有意に改善(11.53ヵ月 vs. 6.47ヵ月)したことが発表され、再発・難治性多発性骨髄腫の新たな治療選択肢になるであろうことが示唆された。
第lll相COLUMBA試験の結果で、Darzalexの皮下投与は静脈内投与に対して非劣性を示し、また皮下投与では投与時間が短縮され、患者への負担も軽減されると報告された。Darzalexは未治療の多発性骨髄の適応は現在申請中となるが、抗モノクロナール抗体が多発性骨髄腫において今後どのように使用されるかが注目される。 (YK)

Oracle Life Sciences オンコロジースペシャリストのレポート
Day three of ASCO 2019 saw a showdown between two anti-CD38 compounds in multiple myeloma, Janssen’s Darzalex and Sanofi’s isatuximab.
