2月13日から3日間に渡り米国サンフランシスコでASCO-GU 2020 (米国臨床腫瘍学会/泌尿器癌シンポジウム)が開催されました。今回のSynix Oncology Newsletterでは、Oracle Life Sciencesコンサルタントが注目した講演トピックをお届けします。
INSTILADRIN®、BCG療法不応性ハイグレード筋層非浸潤性膀胱がんの新たな治療選択として期待
Oracle Life SciencesのQi Fuがサンフランシスコで開催されたASCO-GU 2020からお伝えします。
BCG療法¹不応となったハイグレード筋層非浸潤性膀胱がん(NMIBC)患者を対象に、INSTILADRIN® (nadofargene firadenovec)による膀胱内注入療法の安全性と有効性を評価した第lll相試験の結果がStephen A. Boorjian氏から発表されました。
発表では、上皮内がん(CIS)群の完全奏効率(CR)は53.4%(95%信頼区間:43.3-63.3)、CRを達成した患者は全員が3ヶ月以内の早期奏効であり、12ヶ月時の完全奏功率は24.3%で持続的な奏功であったことが報告されました。ハイグレード群における完全奏功率は、3ヶ月時で72.9%、12ヶ月時は43.8%でした。また有効性だけではなく安全性においても良好な結果を示しており、両群においてグレード3以上の有害事象は3.8%でした。
1:BCG (ウシ型弱毒結核菌)膀胱内注入療法
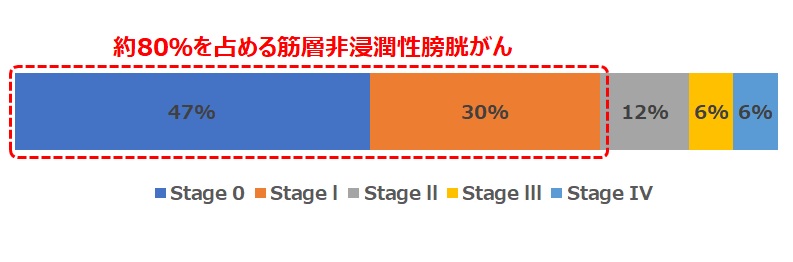
膀胱がん全体の約80%を占める筋層非浸潤性膀胱がん(NMIBC)
NMIBCは膀胱がん全体の約80%を占めており、標準治療は経尿道的膀胱腫瘍切除術(TURBT)となりますが、切除後も再発を繰り返しやすく、術後再発予防を目的としてBCG療法、抗がん剤の膀胱内注入療法が行われています。初期治療および経過観察の目的は、膀胱内再発、筋層浸潤性膀胱がんへの病期進展を防ぐことにあり、治療方針は再発リスク別に決定します。
膀胱がん 罹患患者数(2020)
Data Source: Patient Metrics Japan – Bladder
BCG療法不応は予後不良因子
INSTILADRIN®の有効性・安全性を評価した本試験では、BCG療法不応性ハイグレードNMIBCが対象となっています。BCG療法不応性の定義は、BCG療法開始後12ヶ月以内に再発したBCG療法難治性NMIBC、CRを達成するも12ヶ月以内にCIS再発、6ヶ月以内にTa/T1再発したNMIBCとしています。BCG不応性は再発・進行のリスクが高く、抗がん剤の膀胱内注入の効果も期待できないため、これまで膀胱全摘出術が勧められていました。しかしながら、手術を望まない患者や手術不応の患者が多く、有効的な治療法は不足しています。
米国では免疫チェックポイント阻害剤が治療選択肢に
米国では、2020年1月にKEYTRUDA®がBCG療法不応性な高リスクNMIBCの治療薬として承認されました。ピボタル試験となった第ll相KEYNOTE-057試験(NCT02625961)では、CISまたはCIS+乳頭状腫瘍のある高リスクNMIBCを対象にKEYTRUDA®の有効性・安全性が検討され、CRは41%(95%信頼区間:31-51)、グレード3以上の有害事象は12.6%の患者で確認されました。
INSTILADRIN®は既にFDA(米食品医薬品局)よりBLA(生物製剤承認申請)を受理しており、優先審査品目に指定されています。今回のINSTILADRIN®の第lll相試験の結果は、KEYTRUDA®と直接比較することはできませんが、有効性・安全性において良好な結果を示していることから、今後INSTILADRIN®がKEYTRUDA®に次いで新たな治療選択肢を提供することが期待されます。
※動画配信は終了しました(2021年12月)
