10月24日~10月26日に第57回日本癌治療学会学術集会が福岡にて開催されました。ゲノム医療や分子標的薬をはじめとする個別化医療が進む中、「社会と医療のニーズに応える」のテーマのもと、活発な議論が行われました。数ある演題の中、今回サイニクスが注目したトピックをお届けします。
Topics
- がんゲノム医療で進む個別化医療、「社会と医療のニーズ」ー
- 尿路上皮がん:免疫療法の時代から分子サブタイプ
がんゲノム医療で進む個別化医療、「社会と医療のニーズ」
本学会のテーマは 『社会と医療のニーズに応える』であったが、より最適な治療アクセスの向上を目指す医療現場と、医療財政的な課題を抱える社会といった構図があるが、その一つの表れとして、今年6月に保険適用となったがん遺伝子パネルの使用に関して、両側面からの議論がなされた。
医療従事者としては、 『現状のがん遺伝子パネルは、標準治療終了もしくは希少がんでの使用条件となっていて、適切な治療アクセスの向上を目指す上で、初回治療時の検査が必要』という訴えがあるなか、厚労省としては、『医療経済上のメリットと医療財政面での実効性を考慮する必要があり、現状、初回治療時からの保険適用は難しい』といった見解が出された。今後も、本学会のテーマである医療・社会の両側面からの最適化は引き続きの検討事項となった。
尿路上皮がん(膀胱がん):免疫療法の時代から分子サブタイプ
日本における尿路上皮がん(膀胱がん)の疫学
尿路上皮がんは、尿路(腎盂、尿管、膀胱、尿道)に発生するがんで、最も発生頻度が高いのは膀胱がんとなる。また、高齢者になるほど多くなるがんで、膀胱がんの罹患患者の年齢別割合データでは、65歳以上の患者群が全体の約85% (その約半分が80歳以上) を占めている。高齢化が進む日本で、今後も患者数が増加するがん種の一つと言える。また、転移再発(Stage IV)の割合は、罹患患者数全体の約6%で、再発患者数を含むと約9%程度と推計されている。(CancerMPact – Patient Metrics Japan)
日本における標準治療
現在、日本において進行再発膀胱がんの1st line治療は、ゲムシタビン+シスプラチン併用療法(GC療法)が第一選択となっている。

CancerMPact – Patient Metrics Japan(Bladder) 2018
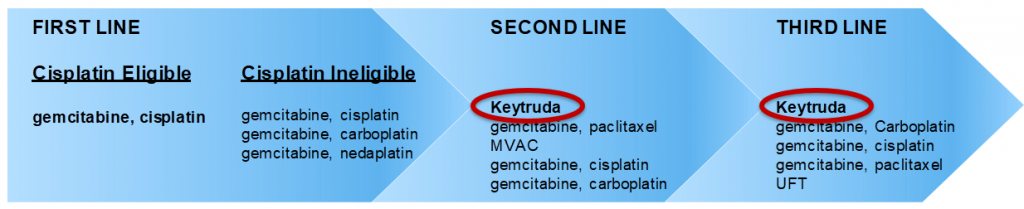
2017年12月 抗PD-1抗体 キイトルーダ®の登場
尿路上皮がんの薬物治療は30年近くの間停滞期にあり、白金製剤を用いた全身化学療法を超える治療の出現がなかったが、2017年12月に免疫チェックポイント阻害剤・キイトルーダ®が日本でも承認された。弊社の2018年7月調査では、2nd lineで約30% 、 3rd lineで約35%の患者に対してキイトルーダ®が使われ、急速に2nd line以降の標準治療となった。
CancerMPact – Patient Metrics Japan(Bladder) 2018
免疫チェックポイント阻害剤 PD1/PD-L1のバイオマーカーの同定が大きな議論
キイトルーダ®はKEYNOTE-045試験にて生存率の延長を示した一方で、テセントリク®の二次治療の試験の一つ IMvigor210では、主要評価の奏効率は達成したものの、全生存率を主要評価とするIMvigor211の試験失敗例について、今年の日本癌治療学会の議論に挙がった。腫瘍遺伝子変異量(TMB)と抗PD-L1抗体の奏功率結果の相関に関するYarchoan M et al. N Eng J Med 2017 Dec 21;377(25):2500-2501の結果が示された上で、本学会ではCD8陽性T細胞などの免疫細胞の腫瘍細胞への浸潤度合も奏効率に関連する可能性も示唆された。
尿路上皮がんの今後の薬物治療
- 早い段階での抗PD-1/PD-L1抗体薬の使用
日本においては、化学療法後に増悪した根治切除不能な尿路上皮癌のみにキイトルーダ®が使用可能だが、会場での臨床医の意見としては、『やはり全身状態 & 免疫状態が良い段階で、抗PD-1/PD-L1抗体薬を使い、治癒にもっていける患者群を増やしたい』という意見が出ていた。一方で、 抗PD-1/PD-L1抗体薬の効果を高めるためには、従来の殺細胞性抗がん剤で、しっかり抗原提示を行ってからの抗PD-1/PD-L1抗体薬の導入意義についても議論がなされていた。 - 抗PD-1/PD-L1抗体薬の使用後の治療
現状、抗PD-L1抗体薬の治療ベネフィットを得られる患者群は未だ少なく、 抗PD-L1抗体薬使用後の治療に関しては、引き続きアンメット・メディカル・ニーズが高い。その中、尿路上皮がんの領域でも、抗体-薬物複合体 (ADC: Antibody-Drug Conjugate)の開発についても注目された。その一つ、エンホルツマブ ベドチンは、白金製剤および PD-1 または PD-L1 阻害剤による治療歴のある局所進行性または転移性尿路上皮がん患者を対象に、第 II 相試験(EV-201 試験)に基づき、2019年7月にFDAに承認申請を行っている。
また、本学会では、先月のESMO 2019の発表からTrop-2をターゲットするADC薬剤についても触れられた。 - 分子サブタイプでの研究
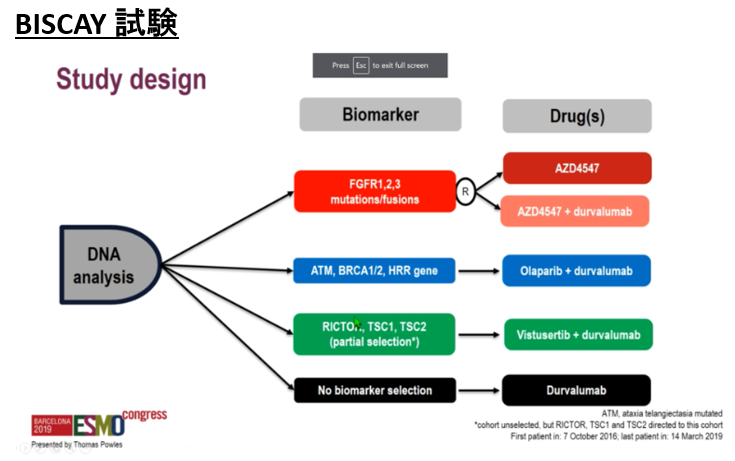
本学会では、先月のESMO 2019のバイオマーカー・プラットホームをベースとするBISCAY試験の結果が示された。 本試験は、バイオマーカー・テストをもとに、患者群を4つに層別し、 抗PD-L1抗体薬・イミフィンジ®と分子標的薬の併用、もしくは各単剤使用での効果をみたPh Ib試験となる。今後、尿路上皮がんの治療においても個別化医療が期待される
最後に
サイニクスは今後も現在および今後の市場動向を注視し、製薬企業の皆さまの市場評価のパートナーとして活動してまいります。今回の日本癌治療学会学術集会で発表された内容も含め、尿路上皮がん(膀胱がん)の概要(疫学情報・標準治療・最近の動向など)をまとめたスライドのご用意もござまいます。ご希望の方は弊社までお問い合わせください。なお、スライドのご提供は製薬企業様のみとさせていただいております(2020年5月26日追記)。