今回のSynix Oncology Newsletterでは、スペイン バルセロナで開催されたESMO 2019 (欧州癌腫瘍学会議)より、パートナーであるOracle Life Sciencesのオンコロジー・コンサルタントが特に注目した臨床試験結果をご紹介します。
オンコロジースペシャリストのレポートはこちらから!
転移性前立腺がん (mCRPC) / 第Ⅲ相 PROfound 試験
バイオマーカーベースの承認? PARP阻害剤の台頭が始まる

Lynparzaは乳がんや卵巣がん患者においてベネフィットを示すことが示されてきましたが、今年のESMOで発表されたグローバル第Ⅲ相PROfound試験では、転移性去勢抵抗性前立腺がん(mCRPC)においても治療ベネフィットがあることを示しました。
PROfound試験は、ZytigaやXtandiなどの新規ホルモン薬での治療後に増悪し、相同組換え修復(HRR : Homologous Recombination Repair)に関連する15の遺伝子のうちのいずれかに変異のあるmCRPC患者を2コホートに分け、LynparzaとZytiga + prednisoneまたはXtandiの併用レジメンの安全性と有効性を比較した試験となります。コホートAはBRCA1、BRCA2、またはATM変異を持つ患者群、コホートBは他のHRR関連遺伝子の変異を持つ患者群でした。
8月にアストラゼネカとMSDがPROfound試験で主要評価項目の画像診断に基づく無増悪生存期間(rPFS)をコホートAで達成したと公表。今回のESMOでは、その結果が発表されました。結果に加え、コホートAは複数の治療を経た患者群であることが注目を惹きます。
発表された結果はコホートAのrPFSが7.39ヵ月(Lynparza群)対3.55ヵ月(対照群)で奏効率は33.3%対2.3%、全患者群ではrPFSが5.82ヵ月対3.52ヵ月というものでした。全生存期間(OS)は未成熟ながら、コホートAと全患者群の双方で3カ月の改善が見られました。全体としてこれまでの治験と同様の安全性がPROfound試験で見られたものの、非致死性の肺動脈塞栓症がLynparza投与群の4.3%において観察されました。
興味深い点として、PROfound試験の対照群がプラセボ群と比較した場合で想定されるのと同様の効果を見せているとパネル参加者からコメントがありました。CARD試験でも同様の結果が報告されており、XtandiとZytigaをシーケンスで使うのは効果的でない可能性が示唆されています。
前立腺がんに対しLynparzaが承認されれば、前立腺がんで初のPARP阻害剤、かつアンドロゲン受容体以外のパスウェイをターゲットとする初の分子標的薬となります。また、PROfound試験を基に承認された場合、前立腺がんで初のバイオマーカーに基づいた承認ともなります。
mCRPC の1stラインでは、Lynparza+Talzenna併用、Zejula+Zytiga併用の開発が進行中。後期ラインではRubraca単剤とLynparza + Keytruda併用の開発が進行しており、前立腺がんでのPARP阻害剤の開発は始まったばかりです。これらの治験はすべてバイオマーカーで患者の絞り込みを行っており、今後どのPARP阻害剤が台頭するか注目が続きます。
膀胱がん / 第Ⅲ相 IMvigor130試験
膀胱がんのパラダイムシフトは今後のデータ次第

今年8月、Rocheは局所進行または転移性尿路上皮がんの1stラインでTecentriq + プラチナ化学療法の併用を検証した第Ⅲ相IMvigor試験が主要評価項目の一つ、PFSの改善を達成したと発表しました。今年のESMOでは結果に対し幾つかの疑問点が取り上げられました。
IMvigor130試験の結果を見ると、Tecentriq + cisplatinまたはcarboplatin + gemcitabineレジメンが膀胱がん1stラインの「治療パラダイムを変える」結果を出したと謳うにはしばらく待つ必要がありそうです。PFSを2カ月延長(Tecetriqレジメン投与群8.2ヵ月対プラセボレジメン投与群6.3ヵ月)と、統計的に優位な結果を出したものの、奏効率は同程度であり、各アームの患者群には問題となる偏りも見られました。特に目を惹いたのは、試験群でシスプラチン適応患者に比べ、シスプラチン不適応患者が多かった点です。試験群、対照群ともにPD-L1発現なし、もしくは低発現の患者が大半を占めていましたが、探索的データ解析の結果を見るとPD-L1発現はPFSの改善に寄与しなかった模様です。
全生存期間中央値(mOS)はTecentriq投与群が統計的に優位な結果を示し、Tecentriq + 化学療法群で16ヵ月に対し、化学療法レジメン群ではわずか13.4ヵ月でした。ただしこのOSデータは中間解析結果であり、パネル参加者からは臨床的意義を持つにはより大きなベネフィットを示す必要があることが強調されました。
現在MSDも同様の試験デザインでKEYNOTE-361試験を進めており、そのデータが2020年に報告される予定です。IMvigor130試験のPFSデータをこのタイミングで発表した背景には、Keytrudaに煎じて有利なマーケティングポジションを獲得したいという戦略の表れと読めます。Keytrudaは、特に米国において、既にPD-L1陽性の1stラインで浸透しているため、RocheとしてはOSが臨床的に有意に改善されることを願うしかない状況となっています。
統計的には幸先のいい結果を示しつつも、今回発表されたデータは「答え」よりも「疑問」を多く提示する結果となりました。Tecentriq + 化学療法レジメンについて、膀胱がん1stラインでの患者選択におけるPD-L1発現の意義はより成熟したデータが必要となりそうです。
前治療歴のないCLL患者群リプルネガティブ乳がん / 第3相Keynote-522試験
早期TNBCに免疫チェックポイント阻害剤の登場? Keytruda併用でpCRを有意に改善

今年のESMOでは、早期ステージのトリプルネガティブ乳がん(TNBC)におけるKeytrudaの有効性を評価した第Ⅲ相KEYNOTE-522試験から中間解析の発表があり、病理学的完全奏功 率(pCR) に有意な改善が示されたことが報告されました。
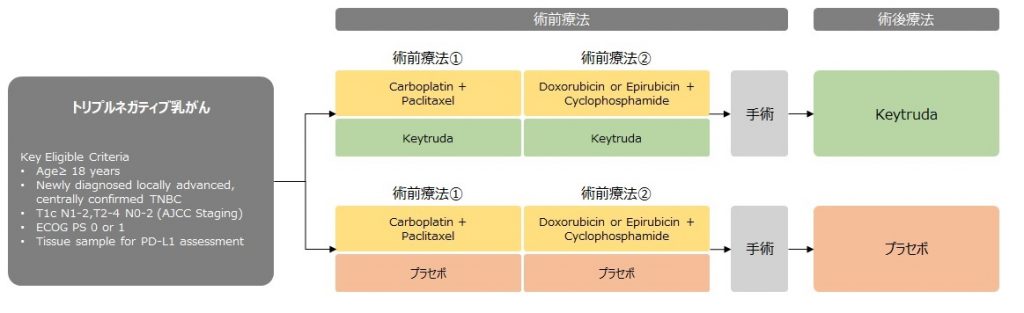
KEYNOTE-522試験はTNBCを対象とし、術前化学療法にKeytrudaを併用し、術後にKeytrudaを投与する試験デザインとなり、主要評価項目はpCR (病理学的完全奏功率)、EFS(無イベント生存率)となっています。今回のESMOにて、Keytruda投与群におけるpCRが64.8%、プラセボ群の51.2%と、有意な改善が示されたことが報告されました。
またpCRはPD-L1発現に関わらず改善が認められ、サブグループ解析におけるPD-L1陽性群(全体の84%)のpCRは、Keytruda投与群で68.9%、プラセボ群で54.9%、PD-L1陰性群はKeytruda投与群で45.3%、プラセボ群で30.3%となり、両群共にベネフィットが見られています。
追跡期間が短いためEFSの最終的な結果は出ていませんが、現時点ではKeytruda投与群で91.3%、プラセボ群で85.3と良好な傾向を示しています。Grade 3以上の有害事象は、両群で大差なかったものの、投与中止に至った有害事象の発生率はKeytruda投与群で23.3%、プラセボ群で12.3%と2倍近くの差が確認されています。またKeytruda投与群においては、急性輸液反応(infusion reaction)、発疹、内分泌障害(甲状腺機能亢進症、副腎機能不全)がプラセボ群に比べて頻度が高い傾向も確認されました。
第3相KEYNOTE-522試験は早期ステージのTNBC 術前・術後療法におけるKeytrudaを評価した初めての試験となり、標準治療が確立されていないこの領域においてKeytruda承認に高い期待が寄せられています。
